燃料電池は,天然ガスや水素などの燃料を,イオンを通す隔膜(電解質膜)を介して空気中の酸素と反応させ,化学エネルギーから直接電気エネルギーを得るエネルギー変換器です。電解質の種類によって
◯ アルカリ形燃料電池(Alkaline Fuel Cell: AFC)
◯ リン酸形燃料電池(Phosphoric Acid Fuel Cell : PAFC)
◯ 溶融炭酸塩形燃料電池(Molten Carbonate Fuel Cell : MCFC)
◯ 固体高分子形燃料電池(Polymer Electrolyte Fuel Cell: PEFC
または Proton Exchange Membrane Fuel Cell: PEMFC)
◯ 固体酸化物形燃料電池(Solid Oxide Fuel Cell : SOFC)
などが開発されています。
燃料電池の発電のしくみ 〜 火力発電との違い
燃料電池は火力発電より「原理的に効率がよい」と言われることがありますが,これは本当でしょうか?
- 火力発電では燃料は一気に燃焼
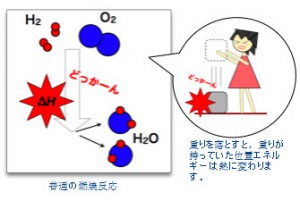
水素やメタンなどの燃料は,空気中の酸素と反応すると爆発的に燃焼して,水や二酸化炭素になります。これは,燃料と酸素が別々に存在する状態よりも,結合したほうが安定なためで,このとき反応前後の違いに相当するエネルギー(*)を,熱として放出します。
火力発電では,この熱でタービンを回して発電します。熱機関は,高温THで熱を吸って低温TLで熱を吐きだすことで連続して動きますが,このときのエネルギー変換効率は,(TH – TL)/TH (カルノー効率)を越えることはできません。
(*) 一定圧力のもとでの発熱量はエンタルピー変化 ΔHで表されます。
これに対し 燃料電池では,燃料と酸素を「電解質」を介して「少しずつ」反応させます。空気極から酸素が取り込まれると,同じだけの酸素が燃料極で燃料と反応します。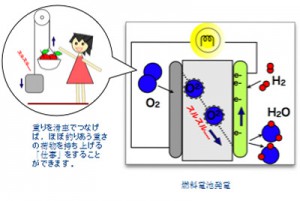
(空気極) 1/2 O2 + 2 e- => O2-
(燃料極) O2- + 燃料 => 生成物 + 2 e-
燃料極で生じた電子は空気極に移動しようとしますが電解質は電子をほとんど通しません。このとき,もしも外部回路が繋がっていなければ反応の駆動力に相当するエネルギーの電子が電極に溜まった状態で反応が止まります。
外部回路を繋いで釣り合いの状態を崩してやると,化学反応の駆動力の一部が外部に取り出されるわけです。
このとき,なるべく釣り合いに近い状態で反応させてやったほうが,化学反応のエネルギーを有効に電気に変換できることになり,釣り合いからずれた分は熱エネルギーとなって放出されます。
(乾電池や蓄電池も基本的には同じ原理です。)
反応の駆動力
燃料電池の反応の駆動力は上に述べたように燃焼反応前後のエネルギーの差です。
少し細かいことを言うと,燃焼反応時のエネルギーの変化分のうちいくらかは,必ず熱として出入りする部分があります。例えば,水素を燃料とした場合,
2H2 + O2 => H2O
のように,反応によって気体分子の数(状態の数,エントロピー)が減少しますが,これらの分子の熱振動として蓄えられていたエネルギーは熱としてしか取り出せません。残りの部分が外部に仕事として取り出し得るエネルギーで反応の駆動力(ΔG)となります。
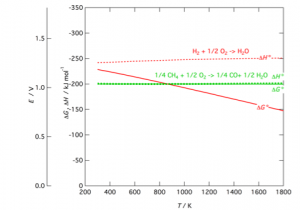
右の図は,水素,メタンを燃料としたときの発熱量(ΔH)と電気エネルギーとして取り出し得る量(ΔG)を温度に対してプロットしたものです。
(すべてのガスが0.1MPaであるとしたときの値:水素とメタンの,0.1MPaでの燃焼熱(ΔH°)と反応の駆動力(ΔG°))
発電効率
燃料電池の単セルの発電効率は,外部に取り出した電力W を供給した燃料mモルの発熱量 m・ΔHで割ったものです。
η = W / (m・ΔH)
外部に取り出した電圧 Vext,電流 Iextで表すと
η = (Vext ・ Iext) / (m・ΔH)
有効に使われた燃料の割合(燃料利用率)Uf = n F Iext / m を使うと
η = Uf nF Vext / ΔH
(ただし,nはmモルの燃料の燃焼に相当する電子数,Fはファラデー定数)
実際に燃料電池発電を行わせると,電流を取り出すにつれて外部に発生する電圧が小さくなります。これは電解質の抵抗や電 極反応に伴う抵抗あるいはセル間接続や配線の抵抗等,諸々の原因によって電池内部でロスが生じるためです。さらにシステムにおいては空気ブロアや水ポンプ など補器類に使用される電力,および直流を交流にする際のロスも差し引く必要があります。
註) 分母のΔHは,LHV基準とHHV基準の2通りがあるので,注意が必要です。LHVは生成した水について水蒸気が生成するまでのエネルギー変化 (Lower Heating Value),HHVは水の凝縮熱も含めて計算したもの(Higher Heating Value)です。HHVのほうが効率の表示値が小さくなります
SOFCの発電効率
上のグラフをみると,水素を燃料とした場合の燃料電池の最大効率は温度が低いほうが高くなることに気づくでしょう。では高温で動作するSOFCは100°C以下で動作するPEFCにくらべて効率が低いのでしょうか?
効率を決めるのは上で述べたように,実際に発生している電圧です。低温形の燃料電池では,電極反応に伴う電極抵抗が大き くなりがちで,通常,開回路の状態でも理論起電力は得られません。また,少し電流をとったところで大きく電圧が降下し,結局0.8V以下でないと十分な電 流がとれません。一方,SOFCでは,電極反応がスムーズで,理論起電力からの電圧降下も比較的直線的です。さらに,メタンなど,化石燃料を使った場合に は,水蒸気改質反応
CH4 + H2O => CO + 3H2
に必要な熱を自身の排熱で賄うこともでき,さらに効率が良くなります。
火力発電より効率が良い?
現在,国内の家庭用コジェネレーション用SOFCは0.7kWのもので,定格で約45-50%(LHV)程度の発電効率です。もう少し大きな2kW のシステムでは60%(LHV)を越えるものも開発されています。 天然ガスを使った最新のコンバインドサイクルによる火力発電の効率も約60%LHVと言われていますが,10kW以下の小さなシステムでこれだけの効率を 出せるということは,火力発電の常識からは考えられないことです。さらに,発生した熱を使ってお湯などに利用すればエネルギーの無駄はさらに小さくなりま す。実際はこのような小さなコジェネレーション(電気-熱併給)システムでは,電気やお湯の需用とのマッチングで実効的な効率が大きく変動しますが,うま く使えば非常に大きな省エネ効果を生み出せるシステムがSOFCです。